किसी विलियन की अम्लता या क्षारीयता या फिर उदासीनता को मापने के लिए एक प्रकार का स्केल का प्रयोग किया जाता है | वह स्केल ही pH स्केल कहा जाता है | एस.पी.एल. सोरेनसन (S.P.L Sorenson) नामक एक वैज्ञानिक ने pH स्केल को बनाया | जिसका उपयोग अम्ल क्षार और लवण के बारे में जानने के लिए करते हैं |

आइये अब देखते है pH स्केल के बारे में |
pH स्केल, बफर सॉल्यूशन, एसिड बेस इंडिकेटर, pH scale kya hai in Hindi:
आज के लेख में हम जानेंगे कि pH स्केल क्या है? pH value क्या होता है ? pH value का महत्त्व क्या है ? बफर सलूशन क्या होता है? इसके प्रकार के बारे में | इंडिकेटर क्या होते है ? कितने प्रकार के इंडिकेटर होते हैं ? उनका इस्तेमाल कहाँ किया जाता है ?
चलिए जानते है सभी टॉपिक के बारे में विस्तार से |
pH scale kya Hai in Hindi:
यह pH स्केल किसी भी विलियन में मौजूद हाइड्रोजन मापने का एक मापक स्केल है जिसका उपयोग किसी भी विलियन की अम्लीयता और क्षारीयता मापने में किया जाता है , pH स्केल कहलाता है |
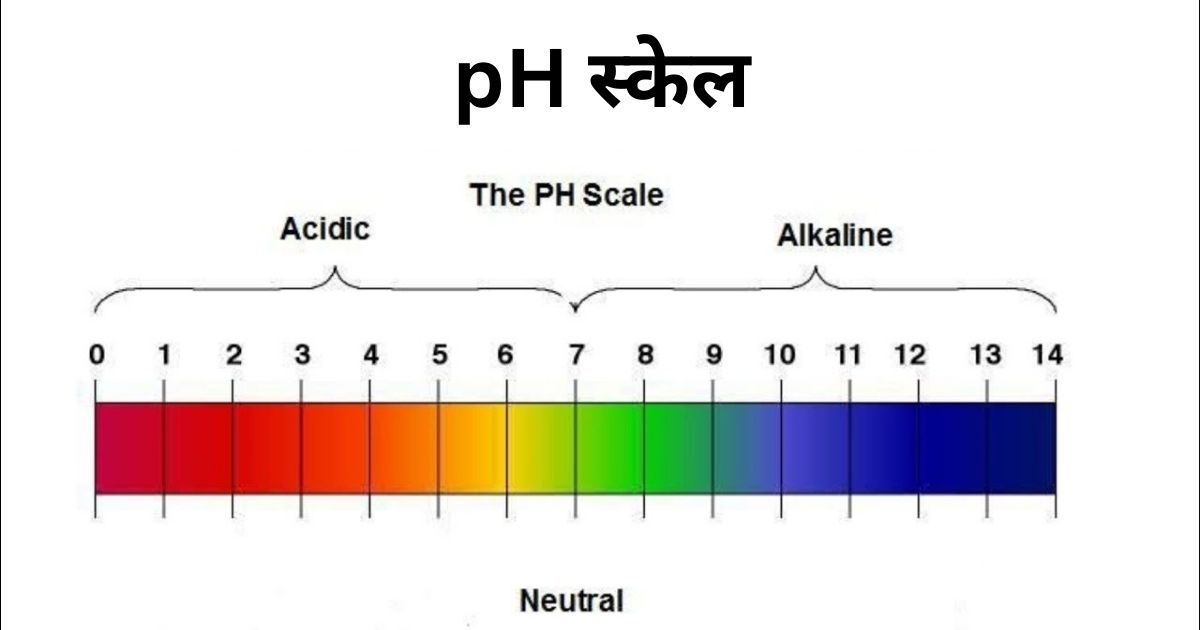
pH का Full Form- Potential of Hydrogen होता है |
किसी विलियन कि अम्लीयता या क्षारीयता को व्यक्त करने के लिए pH स्केल का प्रयोग किया जाता है |
pH = – log[H+] = log 1/ [H+] or log 1/ [H3O+]
किसी विलियन का pH मान 7 से कम हो तो वह विलियन अम्लीय होता है | और जब किसी विलियन का pH मान 7 से अधिक होने पर वह विलियन क्षारीय होता है |
हमारा शरीर 7.0 से 7.8 pH रेंज के बीच कार्य करता है | जीवित प्राणी केवल इसी रेंज में ही जीवित रह सकता है |
वर्षा के जल का pH मान जब 5.6 से कम हो जाता है तो वह अम्लीय वर्षा कहलाती है |
pH मान (pH value) की परिभाषा क्या है? What is the definition of pH value?:
किसी विलियन में हाइड्रोजन आयनों के सांद्रण के व्युत्क्रम के लघुगणक को उस विलियन का pH मान (pH value) कहते हैं |
pH मान किसी पदार्थ की अम्लता या क्षारकता का माप है। किसी विलयन में हाइड्रोजन आयन की सांद्रता को मापने के लिए जिस पैमाने का उपयोग किया जाता है, उसे pH स्केल कहते हैं।
किसी भी विलियन का pH मान हाइड्रोजन आयन (H+) की सांद्रता के व्युत्क्रम के लघुगणक (logarithm) की संख्या के बराबर होता है|
इसलिए,किसी भी विलियन का pH मान हाइड्रोजन आयन के नकारात्मक लघुगणक (negative logarithm) के रूप में लिखा जाता है |
pH= – log 1/ [H+]
= log1[H+]
वैसे तो pH value एक संख्या होती है , जो विलयन या पदार्थो की अम्लीयता व क्षारीयता को प्रदर्शित करती है|
अर्थात जिस विलयन या घोल में जितने कम हाइड्रोजन के आयन होंगे उस घोल की pH मान (pH value) उतनी ही अधिक होंगी |
किसी भी विलियन या घोल का pH मान विलयन में उपस्थित हाइड्रोजन आयन की सांद्रता को दर्शाता है |
अतः pH Value का उपयोग करके यह पता किया जा सकता है कि किसी भी विलयन या पदार्थ में कितने हाइड्रोजन आयन उपस्थित है |
और उसी हाइड्रोजन आयन को calculate कर के यह भी पता किया जा सकता है कि उस विलियन की प्रकृति अम्लीय है या क्षारीय है |
pH स्केल की रेंज कितनी होती है ?
किसी pH स्केल के मान की परास (range) 0 से 14 होती है।
यदि किसी विलयन का pH मान 7 से कम है तो वह अम्लीय प्रकृति का होता है
और यदि किसी विलयन का pH मान 7 है तो वह उदासीन प्रकृति का होता है |
तथा, यदि किसी विलयन का pH मान 7 से अधिक है तो वह क्षारीय प्रकृति का होता है।
pH स्केल की खोज किसने की ? pH के अविष्कारक कौन हैं? Who discovered the pH scale? Who is the inventor of pH? :
सन 1909 ई. में डेनमार्क के बायोकेमिस्ट एस.पी.एल. सोरेनसन (S.P.L Sorenson) ने pH स्केल बनाया |
जो किसी जलीय विलियन के H+ आयन की सांद्रता बताने वाला एक स्केल था ,जिसे pH वैल्यू निकालने वाले pH स्केल के रूप में जाना जाता है|
किसी भी विलियन का pH एक संख्या होता है जो उस विलियन की अम्लीयता या क्षारीयता के बारे में बताता है |
Basic concept of pH value pH मान की मूल अवधारणा क्या है?:
pH मान की अवधारणा एक जलीय या तरल घोल की उदासीनता, अम्लीयता और क्षारीयता की एक माप है |
आइये ये निम्नलिखित हैं|
pH of acidic solution अम्लीय घोल का pH:
सभी अम्लीय विलियन या घोलों का pH मान 7 से कम होता है|
pH value < 7
- अतः जब कभी किसी घोल का pH 7 से कम हो तो वह अम्लीय प्रकृति का होगा|
- यह अम्लीय विलियन, नीले लिटमस को लाल रंग में बदल देगा |
- येअम्लीय घोल, मिथाइल ऑरेंज को गुलाबी रंग का बना देगा |
- यह अम्लीय घोल, फेनॉल्फथलीन को रंगहीन कर देगा |
pH of alkaline solution क्षारीय घोल का pH:
सभी क्षारीय विलियन या घोलों का pH मान 7 से अधिक होता है|
pH value > 7
- अतः जब कभी भी किसी घोल के pH का मान 7 से अधिक हो तो वह क्षारीय प्रकृति का होगा |
- यह क्षारीय घोल, लाल लिटमस को नीले रंग में बदल देगा |
- ये क्षारीय घोल, मिथाइल ऑरेंज को पीला रंग में बदल देगा |
- यह क्षारीय विलियन, फिनॉल्फथलीन को गुलाबी रंग का बना देगा |
pH of neutral solution (pure water) उदासीन घोल (शुद्ध पानी) का pH :
शुद्ध पानी का pH 7 होता है|
pH value = 7
- जब कभी एक विलियन का pH 7 हो, तो वह उदासीन घोल होगा|
- ऐसा विलियन किसी भी लिटमस पत्र या विलियन या किसी अन्य संकेतक पर कोई प्रतिक्रिया नहीं करेगा |
दैनिक जीवन में pH का महत्व Importance of pH in everyday life:
हमारे दैनिक जीवन में pH का बहुत महत्त्व है | ये निम्नलिखित हैं |
1)जीवित पौधे और जानवरों में In living plants and animals :
पौधे और जानवर pH value के प्रति संवेदनशील होते हैं।
हमारा शरीर pH value 7.0 से 7.8 के दायरे में काम करता है।
जीवित जीव pH value परिवर्तन की एक सीमित सीमा में ही जीवित रह सकते हैं।
2) अम्लीय वर्षा में In acid rain:
अम्लीय वर्षा के कारण जब नदी के पानी का pH value 5.6 से कम हो जाता है ,
तो ऐसी नदियों में जलीय जीवन का जीवित रहना मुश्किल हो जाता है।
पौधों को उनके स्वस्थ विकास के लिए एक विशिष्ट pH value की आवश्यकता होती है।
3) मिट्टी में अम्लता में Acidity in the soil:
उर्वरकों के अत्यधिक उपयोग से मिट्टी अम्लीय हो जाती है जो पौधों की वृद्धि के लिए अच्छी नहीं होती है।
इसलिए मिट्टी को पौधों के लिए उपयुक्त बनाने के लिए कुछ क्षार मिलाया जाता है |
जैसे बिना बुझा चूना (कैल्शियम ऑक्साइड) या बुझा हुआ चूना (कैल्शियम हाइड्रॉक्साइड) मिट्टी में मिलाया जाता है |जो अतिरिक्त अम्ल को निष्क्रिय कर देता है।
यदि मिट्टी अधिक क्षारीय हो जाती है, तो इसमें कार्बनिक पदार्थ (जो अम्ल छोड़ते हैं) मिलाए जाते हैं।
4) पेट या उदर में अम्लता में In stomach acidity:
हमारा पेट हाइड्रोक्लोरिक एसिड पैदा करता है।
यह हाइड्रोक्लोरिक एसिड हमारे पेट को बिना नुकसान पहुंचाए भोजन के पाचन में सहायक है।
अपच के दौरान, पेट में मौजूद ग्रंथियां बहुत अधिक एसिड उत्पन्न करता है और इससे पेट में ऐठन, दर्द और जलन होती है।
इस दर्द से छुटकारा पाने के लिए लोग मैग्नीशियम हाइड्रॉक्साइड (मिल्क ऑफ मैग्नीशिया) जैसे एंटासिड नामक बेस का इस्तेमाल करते हैं।
ये एंटासिड अतिरिक्त एसिड को बेअसर कर देते हैं।
5) दन्त क्षय में In dental caries:
मुंह का pH value 5.5 से कम होने पर दांतों का सड़ना शुरू हो जाता है।
मुंह में मौजूद बैक्टीरिया खाने के बाद मुंह में बची चीनी और खाद्य कणों के अपघटन से एसिड पैदा करते हैं।
टूथ पेस्ट आम तौर पर बेसिक होते हैं, जब हम अपने दांतों को साफ करते हैं ,
तो वे इस अतिरिक्त एसिड को बेअसर कर सकते हैं और दांतों की सड़न को रोक सकते हैं।
6) मधुमक्खी और कीटो के डंक में In bee and insect stings :
चींटी के काटने से या’मधुमक्खी का डंक त्वचा में एक एसिड (आमतौर पर फॉर्मिक एसिड) डालता है जिससे दर्द और जलन होती है।
डंक मारने वाली जगह पर बेकिंग सोडा (सोडियम हाइड्रोजन कार्बोनेट) या कैलामाइन (जिंक कार्बोनेट) जैसे माइल्ड बेस का इस्तेमाल करने से राहत मिलती है।
7) दूध में In milk:
केले के पत्ते की प्रकृति क्षारीय होती है, इसलिए यह खमीर बनने से बचाता है।
इसलिए दूधवाले आमतौर पर दूध के जार में एक केले का पत्ता रखते थे।
8)कृषि में In agriculture:
मिट्टी के pH का निर्धारण कर हम यह जान सकते हैं कि वह अम्लीय है या क्षारीय |
इससे इस्तेमाल किए जाने वाले उर्वरकों और बोए जाने वाले फसलों के प्रकार के निर्धारण में मदद मिलती है |
9)जैविक प्रक्रिया में In biological process:
pH) का पता लगा कर हम किण्वन (fermentation), एंजाइम हाइड्रोलिसिस, कीटाणुनाशन आदि जैसी जैविक प्रक्रियाओँ के माध्यम को समायोजित कर सकते हैं|
10)संक्षारण अनुसंधान में In corrosion research:
समुद्र के पानी का pH माप कर बनाए जाने वाले जहाजों और पनडुब्बियों के लिए इस्तेमाल किए जाने वाली सामग्रियों पर क्षारीय समुद्री जल के प्रभाव का अध्ययन किया जाता है|
11)कारखानों में In factories:
फैक्ट्री या कारखानों में चलने वाले कई एसिड होते हैं, जो अगर जलाशयों में गिरते हैं, तो उन्हें प्रदूषित करते हैं।
अत: अम्ल को उदासीन करने के लिए कुछ क्षारकीय पदार्थ मिलाए जाते हैं।
H+ जलीय आयनों की सांद्रता में परिवर्तन के साथ pH में परिवर्तन (Variation of pH with the change in the concentration of H+ aqueous ions):
ताजा भूजल (fresh ground water) का pH हवा के संपर्क में आने पर थोड़ा कम हो जाता है।
यह हवा में कार्बन डाइऑक्साइड (CO2) की उपस्थिति के कारण होता है जो पानी में घुलकर पानी में घुलकर एक कमजोर एसिड H2CO3 (कार्बोनिक एसिड) देता है।
ये अम्ल H+ आयन प्रदान करता है और इस प्रकार, पानी की अम्लता को बढ़ाता है, जिससे pH कम हो जाता है।
अम्लीय विलयन में क्षार मिलाने पर pH बढ़ जाता है और अम्ल मिलाने पर क्षारकीय विलयन का pH घट जाता है।
यदि एक प्रबल एसिड जैसे HCl, H2SO4, आदि को NaOH (सोडियम हाइड्रॉक्साइड), KOH (पोटेशियम हाइड्रॉक्साइड), आदि जैसे प्रबल क्षार के समान रूप से मिलाया जाता है, तो पूर्ण नयूट्रालाइजेशन होती है |
और pH 7 के साथ एक उदासीन विलियन प्राप्त होता है।
जब अम्ल विलयन में जल मिलाकर तनु किया जाता है तो इसका pH कम हो जाता है |
जैसे- pH 6 के विलयन को तनु करने पर इसका pH कम हो जाता है और अम्लीय बना रहता है।
ऐसा इसलिए होता है क्योंकि पानी में आम तौर पर आयनीकरण बढ़ जाता है।
pH scale से सम्बंधित कुछ महत्वपूर्ण बाते Some important facts related to the pH scale:
- इस स्केल में 0 से लेकर 14 तक अंक होते है यानी स्केल रेंज 0 – 14 होती है |
- ताप के बढ़ाने पर pH का मान घटता है |
- जिस विलयनो के pH का मान 7 से कम होता है वे अम्लीय होते है |
- जिन विलयनो के pH का मान 7 से अधिक होता है वे क्षारीय होते है |
- जिस भी घोल या पदार्थो की pH वैल्यू जितनी अधिक होगी वो उतना ज़्यादा क्षारीय (Base) होगा |
- जिन घोल या पदार्थ की pH वैल्यू जितनी कम होगी वो उतना ज़्यादा अम्लीय (Acid) होगा|
- जिस भी घोल या पदार्थ की pH value 7 pH होंगी वह उदासीन यानी ना तो क्षारीय और ना अम्लीय होगा | उदहारण -शुद्ध जल
- कम pH वाला अम्लीय विलियन उच्च pH मान वाले दूसरे विलियनों कीतुलना में अधिक शक्तिशाली होता है |
जैसे :- 2 pH वाला एक विलियन 5 pH वाले विलियन की तुलना में अधिक शक्तिशाली होता है |
- उसी प्रकार उच्च pH मान वाला क्षारीय विलियन कम pH मान वाले क्षारीय विलियन की तुलना में अधिक शक्तिशाली होता है|
- बहुत अधिक अम्लीय विलियन का pH मान शून्य (0) से कम हो सकता है और बहुत अधिक क्षारीय विलियन का pH मान 14 से अधिक हो सकता है|
pH value of some common substances कुछ सामान्य पदार्थों का pH मान :
बैटरी एसिड = pH value (0 – 1)
पेट का अम्ल = pH value (1.2 – 2.0)
नींबू का रस = pH value (2.2 – 3.4)
सिरका = pH value (2.2 – 3.4)
संतरे का रस = pH value (3.2 – 3.9)
सोडा = pH value (3.2 – 3.9)
कुछ दंत कुल्ला = pH value (3.2 – 3.9)
वाइन = pH value (3.2 – 3.9)
टमाटर का रस = pH value (4.0 – 4.4)
बियर = pH value (4.0 – 4.4)
ब्लैक कॉफी = pH value (4.5 – 5.5)
एसिड वर्षा (acid Rain) = pH value (5.0)
लार = pH value (6.4 – 6.6)
गाय का दूध = pH value (6.4 – 6.6)
शुद्ध पानी = pH value (7)
मानव मूत्र = pH value (7.3 – 7.5)
मानव रक्त = pH value (7.3 – 7.5)
आँसू = pH value (7.4)
समुद्री जल = pH value (8)
बेकिंग सोडा = pH value (9.2)
पीने का सोडा = pH value (9.2)
एंटासिड = pH value (10)
दंत चिकित्सा उपचार = pH value (11)
साबुन का पानी =pH value (12.5)
सोडियम हाइड्रोक्साइड = pH value (14)
इंडिकेटर Indicator संकेतक:
संकेतक घोल में रंग परिवर्तन दिखाते हैं क्योंकि घोल का pH बदल जाता है।
अतः इनका उपयोग यह पहचानने के लिए किया जाता है कि कोई विलयन अम्लीय है, क्षारीय है या उदासीन है।
pH पेपर या यूनिवर्सल इंडिकेटर या pH मीटर का उपयोग करके समाधान का पीएच निर्धारित किया जा सकता है।
जैसे- लिटमस, हल्दी, चीनी गुलाब की पंखुड़ियाँ (गुड़हल), हाइड्रेंजिया, पेटुनिया और जेरेनियम की पंखुड़ियाँ।
एसिड बेस इंडिकेटर Acid Base Indicator (संकेतक):
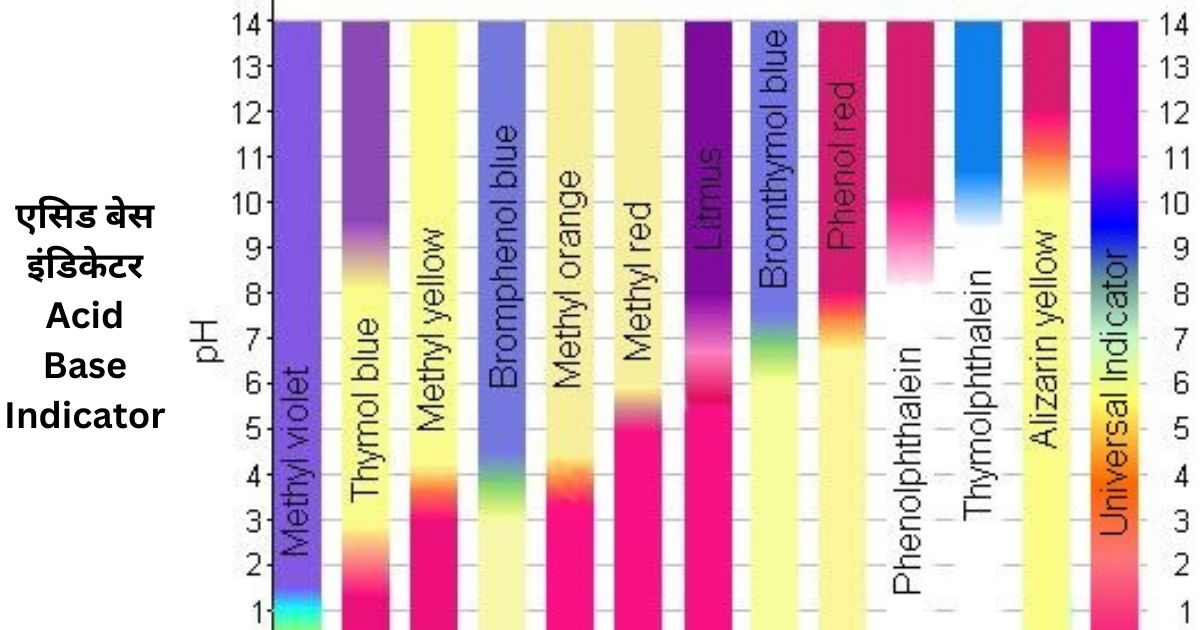
ये या तो कमजोर कार्बनिक अम्ल या कमजोर कार्बनिक आधार हैं।
उदाहरण के लिए, फेनोल्फथेलिन को एक कमजोर कार्बनिक अम्ल माना जा सकता है |
और मिथाइल ऑरेंज को एक कमजोर कार्बनिक आधार माना जा सकता है।
यदि क्षार दुर्बल है तो फेनॉल्फथेलिन उपयुक्त नहीं है और यदि अम्ल दुर्बल है तो मिथाइल ऑरेंज उपयुक्त नहीं है।
विभिन्न माध्यमों में संकेतकों का रंग Colour of indicators in different media:
| Indicators | pH Range | In Basic medium colour | In Acidic medium colour |
| Methyl orange
मिथाइल ऑरेंज |
3.1 – 4.5 | Yellow | Red / Pink |
| Methyl red
मिथाइल लाल |
4.2 – 6.3 | Yellow | Red |
| Phenolphthalein | 8.0 – 9.3 | Pink | Colourless |
| Litmus | 5.5 – 7.5 | Blue | Red |
Buffer Solution बफर विलियन (प्रतिरोधक विलियन/ घोल) :
वे विलयन जो तनुकरण पर या अम्ल या क्षार की थोड़ी मात्रा मिलाकर pH (या अम्लता या क्षारीयता) में परिवर्तन का विरोध करते हैं, बफर विलयन कहलाते हैं।

एक ऐसा घोल जिसमें थोड़ा मात्रा में अम्ल या क्षार के मिलाए जाने से उसके pH में कोई अंतर न आए |
इसका प्रयोग केमिकल एप्लीकेशनों के व्यापक प्रकार में pH को स्थिर मान के करीब बनाए रखने में किया जाता है |
कई जीवन अपेक्षाकृत कम pH रेंज में ही विकसित होते हैं इसलिए वे बफर घोल का प्रयोग pH को स्थिर बनाए रखने में करते हैं |
प्रकृति में, रक्त के pH को नियमित करने के लिए बाईकार्बोनेट बफरिंग प्रणाली का प्रयोग किया जाता है |
सोडियम एसीटेट और एसिटिक एसिड का विलियन प्रभावी बफर विलियन का एक उदाहरण है |
विलियन जिसमें बफर विलियन मिलाया जाता है वह बेहद धीमे अम्ल के तौर पर काम करता है |
बफर विलियन के प्रकार Types of Buffer Solutions:
ये बफर विलियन दो प्रकार के होते हैं।
1) अम्लीय बफर
2) क्षारीय बफर
अम्लीय बफर Acidic Buffer :
यह अम्लीय बफर विलियन समान मात्रा में एक दुर्बल अम्ल और प्रबल क्षार के साथ उसके लवण (salt) को मिलाकर प्राप्त किया जाता है |
उदहारण
1)एसिटिक एसिड और सोडियम एसीटेट का मिश्रण pH 4.75 के आसपास अम्लीय बफर विलियन के रूप में कार्य करता है।
2)बोरिक एसिड और बोरेक्स का मिश्रण अम्लीय बफर का एक और उदाहरण है।
क्षारीय बफर Basic Buffer:
यह क्षारीय बफर विलियन एक दुर्बल क्षार और इसके लवण (salt) को प्रबल एसिड के साथ समान मात्रा में मिलाकर प्राप्त किया जाता है।
जैसे,
1)अमोनियम क्लोराइड (NH4Cl) और अमोनियम हाइड्रॉक्साइड (NH4OH) का मिश्रण पीएच 9.25 के आसपास बुनियादी बफर विलियन के रूप में कार्य करता है।
2)हमारे द्वारा कई अम्लीय भोजन लेने के बावजूद H2CO3 / HCO3- बफर की मदद से रक्त pH को बनाए रखा जाता है।
conclusion:
उम्मीद करते हैं कि आपको यह ब्लॉग पोस्ट पसंद आया होगा | आप इस जानकारी का पूरा से पूरा फायदा उठाये | शेयर करना ना भूलें | यह पोस्ट “pH स्केल, बफर सॉल्यूशन, एसिड बेस इंडिकेटर pH scale kya hai in Hindi” के बारे में था | आप अपने विचार या सुझाव कमेंट बॉक्स में जरुर बताएं | और हमारे साथ जुड़े रहें |
हैप्पी और healthy रहें |
आपका दिन शुभ हो | धन्यवाद |
Related Post: